
 Рисунок
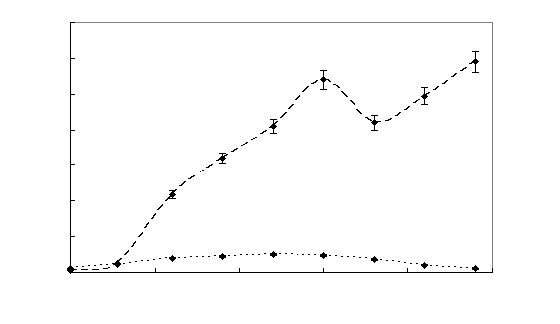
7 – Динамика роста штамма Sm11 в среде, содержащей МФК
Рисунок
7 – Динамика роста штамма Sm11 в среде, содержащей МФК
|
|
|
|

Рисунок 8 – Изменение концентрации МФК
В рассматриваемых системах различают следующие фазы размножения:
лаг-фаза – период между засевом и началом размножения;
экспоненциальная фаза – период размножения микроорганизмов с постоянной скоростью;
фаза гибели – период, в течение которого популяция погибает.
Как видно из рисунка 7, рост культуры на среде, содержащей МФК, начинался после непродолжительной лаг-фазы – не более 10 часов, затем наблюдался значительный рост микроорганизмов. Концентрация МФК уменьшается в 2 раза в течение 40 -45 часов (рисунок 8). После 58 – 62 часов рост культуры и потребление МФК прекращалось, что обусловлено недостатком в питательной среде источника углерода. При добавлении глутамата натрия рост клеток возобновлялся, и наблюдалось дальнейшее уменьшение концентрации МФК.
Для оценки возможности биодеструкции изопропилового, изобутилового и пинаколилового эфиров использовали отобранный ранее штамм Sm11 рода Alcaligenes sp.
Начальная концентрация кислого эфира составляла 0,2 г/л. Рост культур контролировали по изменению оптической плотности. По данным измерений оптической плотности и концентрации загрязнителя строили кривые роста культур и потребления кислых эфиров.
Динамика роста культуры и потребления изопропилового эфира представлена на рисунке 9 и 10.

|
|
|
![]()
|
|

Рисунок 10 – Изменение концентрации изопропилового эфира МФК
Как видно из рисунка 9, рост культуры на среде, содержащей изопропиловый эфир, начинался практически без лаг-фазы, сразу наблюдался значительный рост микроорганизмов. При этом наблюдается уменьшение концентрации изопропилового эфира в 1,6 раза в течение 42 часов (рисунок 10). После 40-50 часов рост культуры прекращался, что обусловлено недостатком в питательной среде источника углерода. При добавлении глутамата натрия рост культуры возобновлялся.
Аналогичная тенденция выявлена и для изобутилового эфира (рисунок 11 и 12).
|
|
|

Рисунок 11 – Динамика роста штамма Sm11 в среде, содержащей изобутиловый эфир МФК
Как видно из рисунка 11, рост культуры среде, содержащей изобутиловый эфир МФК, начинается практически сразу, без лаг-фазы. После 80 часов рост штамма Sm11 прекращается, что обусловлено отсутствием в среде источника углерода. Затем рост культуры возобновляется. Изменение концентрации изобутилового эфира представлено на рисунке 12.

![]()
Рисунок 12 – Изменение концентрации изобутилового эфира МФК
Как показано на рисунке 12, концентрация изобутилового эфира МФК уменьшается в 1,7 раза в течение 70 – 90 часов.
Рост штамма Sm11 рода Alcaligenes sp в среде, содержащей пинаколиловый эфир, и уменьшение концентрации загрязнителя представлены на рисунках 13 и 14 соответственно.
|
|
|

Рисунок 13 – Динамика роста штамма Sm11 бактерий рода Alcaligenes sp


·
![]()
![]()
Рисунок 14 – Изменение концентрации пинаколилового эфира МФК
Как показано на рисунках 13 и 14, рост культуры на питательной среде, содержащей пинаколиловый эфир МФК, также характеризуется непродолжительной лаг-фазой, однако биодеструкция эфира происходит интенсивнее: концентрация пинаколилового эфира МФК уменьшается в 1,7 раза в течение 50 – 70 часов.
На основании полученных данных определяли вес сухой биомассы, удельная скорость роста, экономический коэффициент. Результаты представлены в таблице 6.
Таблица 6 – Основные параметры роста культуры в присутствии метилфосфоновой кислоты и ее кислых эфиров
| Параметр | МФК | изопропило-вый эфир |
изобутило- вый эфир |
пинаколило-вый эфир | |
| Биомасса, г/л | 2,7 | 0,9 | 0,95 | 1,05 | |
|
Максимальная скорость роста, ч-1 |
0,16 | 0,05 | 0,04 | 0,05 | |
| Количество метаболизируемого загрязнителя, мг | лаг-фаза | 25 | 46 | 28 | 20 |
| весь период | 168 | 100 | 102 | 105 | |
|
Экономический коэффициент, мг загрязнителя / г биомассы |
лаг-фаза | 200 | 60,5 | 42,4 | 25,0 |
| весь период | 62 | 55,5 | 53,7 | 50,0 | |
Как видно из таблицы 6, в присутствии кислых эфиров культура Sm11 характеризуется невысокой скоростью роста 0,04 – 0,06 ч-1. Причем рост культуры начинается практически сразу, без лаг-фазы. Рост биомассы прекращался спустя 40-50 часов вследствие полного потребления источника углерода. Об этом свидетельствует тот факт, что после добавочного внесения глутамата натрия рост возобновлялся Для культуры Sm11 отмечается и высокая величина потребления метилфосфонатов в расчете на единицу биомассы. Следует отметить, что экономический коэффициент культуры в лаг-фазе и за весь период отличается незначительно: для изопропилового эфира составляет 60,5 и 55,5 мг загрязнителя/г биомассы соответственно. Однако для пинаколилового эфира данный показатель отличается в два раза и составляет
25,5 и 50,0 мг загрязнителя/г биомассы соответственно. Характерным отличием роста культуры на среде, содержащий пинаколиловый эфир, является более продолжительная лаг-фаза, на протяжении которой метабилизируется меньшее количество эфира – 20 мг по сравнению с 46 мг изопропилового эфира, однако количество поглощенного пинаколилового эфира за весь период выше - 105 мг.
По результатам количественной оценки культур – накоплению биомассы, удельной скорости роста и эффективности разложения соединений с С-Р связью был отобран наиболее активный штамм Sm11 рода Alcaligenes sp.
3.3 Пути метаболизма органофосфонатов
Процессы биодеструкции любых соединений не могут быть оценены без изучения путей метаболизма и механизма их регуляции. Применительно к нашей работе проводится сравнительное изучение механизмов деструкции соединений с С-Р связью.
Штаммы-деструкторы МФК осуществляют расщепление С-Р связи посредством ферментной системы с участием С-Р лиазы, доказательством чему служит обнаружение метана в газовой фазе при культивировании в среде с МФК в количествах, эквимолярных потребленному источнику фосфора:
|

Глифосат метаболизируется через аминометилфосфоновую кислоту (АМФК). Об этом свидетельствует идентификация глиоксилата как продукта расщепления ГФ посредством глифосат-оксидоредуктазы. При реализации этого пути фосфат-ион отщепляется на последующих стадиях при участии фосфонатазы.

МФК и другие фосфонаты выступают в роли прекурсоров фосфат-иона в процессах биодеградации фосфорорганических соединений с участием широкого спектра природных микроорганизмов, находящихся в условиях фосфорного голодания.
Выводы
1 Проведен анализ литературных данных о существующих технологиях реабилитации загрязненных почв. Показано, что биологические методы санации территорий, загрязненных продуктами деструкции фосфорорганических отравляющих веществ, наиболее экологически безопасны, эффективны, экономичны и выгодно отличаются отсутствием вторичных отходов.
2 Проведен скрининг микроорганизмов-деструкторов фосфорорганических соединений. Наилучшая способность к растворению метилфосфонатов отмечается у штамма Sm11, относящегося к роду Alcaligenes sp.
3 Изучена возможность биодеструкции продуктов разложения фосфорорганических отравляющих веществ: метилфосфоновой кислоты и её изопропилового, изобутилового, пинаколилового эфиров. Установлено, что штамм Sm11 рода Alcaligenes sp является активным деструктором метилфосфоновой кислоты и её кислых эфиров: наблюдается уменьшение концентрации метилфосфоновой кислоты в 2 - 2,2 раза в течение 40 -45 часов, кислых эфиров – в 1,6 - 1,7 раза в течение 50 - 70 часов. Показано, что культура характеризуется высокой удельной скоростью роста 0,04 - 0,05 ч-1 как в присутствии метилфосфоновой кислоты, так и кислых эфиров.
Список использованных источников
1. Конвенция о запрещении разработки, производства, накопления и применения химического оружия и о его уничтожении. ООН, Женева, 1993. - 170 с.
2. Федеральный закон РФ № 76-ФЗ от 2 мая 1997 г. (с изменениями от 29 ноября 2001 г., 10 января 2003 г.) «Об уничтожении химического оружия».
3. Федеральный закон РФ № 136-ФЗ от 7 ноября 2000 г. «О социальной защите граждан, занятых на работах с химическим оружием».
4. Федеральная целевая программа «Уничтожение запасов химического оружия в Российской Федерации». Постановление Правительства РФ от № 969 от 29 декабря 2007 г. – М., 2008. – 28 с.
5. Холстов В.И., Тарасевич Ю.В., Григорьев С.Г. Пути решения проблемы безопасности объектов по уничтожению химического оружия // Ж. росс. хим. об-ва им. Д.И. Менделеева. - 1995. - Т.39. - №4. – С. 65-73.
6. Скоробогатова В.И., Щербаков А.А., Мандыч В.Г. Санация загрязненных территорий в районах хранения и уничтожения химического оружия. - Российский химический журнал им. Д.Менделеева. – 2007. – том LI – выпуск 2. – С.71-74.
7. Маршалл В. Основные опасности химических производств. – М.: Мир, 1989. – 672 с.
8. Горский В.Г., Моткин Г.А., Петрунин В.А. и др. Научно-методические аспекты анализа аварийного риска. – М.: Экономика и информатика, 2002. – 260 с.
9. Организация и осуществление санитарно-эпидемиологического надзора на объектах по уничтожению фосфорорганических отравляющих веществ: Методические указания (временные)// Сборник инструктивно-методических документов по проблеме уничтожения химического оружия: Часть II. Фосфорорганические отравляющие вещества: Том 1 / ФУМБЭП при МЗ РФ. – Москва, 2001. - С. 187-243.
10. Правила безопасности объектов по УХО на основе ФОВ. – М.: Российское агентство по боеприпасам, 2003. - С. 66.
11. Радилов А.С., Шкаева И.Е., Николаев А.И. и др. Экспресс-оценка особо опасных химических соединений в объектах окружающей среды// Научно-технические аспекты обеспечения безопасности при уничтожении, хранении и транспортировке химического оружия. Тез. докл. научно-практической конференции. – Москва, 2004. – С. 161-162.
12. Методика определения площади защитных мероприятий, устанавливаемой вокруг объектов по хранению ХО и ОУХО. - М.: МО РФ, 1999. – 98с.
13. Методика расчета концентраций в атмосферном воздухе вредных веществ, содержащихся в выбросах предприятий (ОНД-86). Л.: Гидрометео-издат, 1987. – 111 с.
14. Постановление Правительства РФ «Об утверждении площади ЗЗМ, устанавливаемой вокруг объекта по хранению химического оружия (пос. Марадыковский Кировской области) и перечня населенных пунктов, включаемых в указанную зону от 29.12.2004 № 867. – Москва, 2004. – 5 с.
15. Методика прогнозирования масштабов заражения сильнодейству-ющими ядовитыми веществами при авариях (разрушениях) на химически опасных объектах и транспорте. РД 52.04.253 – 90. Л.: Гидрометеоиздат, 1991. – 56 с.
16. Методика определения площади защитных мероприятий, устанавливаемой вокруг объектов по хранению ХО и ОУХО. - М.: МО РФ, 1999. – 84 с.
1.7 Мурин А.В. Математическое моделирование на параллельных системах последствий химических аварий. – Автореф. Дис. ... канд. физ.-мат. Наук /Ижевск - ИжГТУ, 2002 - 24 с.
18. Тронин С.Я., Мещеряков Е.М., Хромов М.Н. Организация защиты населения при авариях на объектах хранения и уничтожения химического оружия// Ж. росс. хим. об-ва им. Д.И. Менделеева. – 2002. - т. 36. - № 6. - С. 112-117.
19. Сильнодействующие ядовитые вещества и защита от них. Под ред. В.А. Владимирова. – М.: Воениздат, 1989. – 109 с.
20. Евстафьев И.Б., Холстов В.И., Григорьев С.Г. Методические основы оценки аварийной опасности объектов по хранению и уничтожению химического оружия // Ж. росс. хим. об-ва им. Д.И. Менделеева. - 1993. - Т. 37, №3. С.5 0-59.
21. Скоробогатова В.И, Кобцов С.Н., Щербакова Л.Ф., Мандыч В.Г., Сотников Н.В, Щербаков А.А. Особенности поведения фосфорорганических отравляющих веществ в воде и почве - Сборник №5 научных трудов СВИРХБЗ. – Саратов, 2005.- С.152-155.
22. Александров В.Н., Емельянов В.И. Отравляющие вещества. – М.: Воениздат, 1990. – 271 с.
23. Ашихмина Т.Я. Научно-методологические основы системы комплексного экологического мониторинга объектов хранения и уничтожения химического оружия. - Киров.: Вятка, 2001. – 473 с.
24. Савельева Е.И., Зенкевич И.Г., Кузнецова Т.А. и др. Исследование продуктов превращений фосфорорганических отравляющих веществ методом газовой хроматографии – масс-спектрометрии //Ж. росс. хим. об-ва им. Д.И. Менделеева. - 2002. - Т. 46. - №6. – С.89-92.
25. Савельева Е.И., Радилов А.С., Кузнецова Т.А. и др. Определение метилфосфоновой кислоты и ее эфиров как химических маркеров фосфорорганических отравляющих веществ - Журнал прикладной химии. 2001, Т. 74, № 10. - 1677 с.
26. Франке З., Франс П., Варнке В. Химия отравляющих веществ. Т. 1. - М.: Химия, 1973. – 270 с.
27. Скурлатов Ю.И., Дуга Г.Г. Введение в экологическую химию. – Учебное пособие. М.: Высш. Шк., 1994. – 400с.
28. Корте Ф., Бахадир М. и др. Экологическая химия / Пер. с нем. под ред.- Корте. М.: Мир, 1996. - 396 с.
29. Безопасность России: Правовые, социально-экономические и научно-технические аспекты. Региональные проблемы России с учетом риска и возникновения природных и техногенных катастроф// В.И. Осипов, Ю.А. Мамаев, В.А. Королев.- М.: МГФ «Знание», 1999. – 144 с.
30. Орлов Д.С. Химия и охрана почв. М.: Химия, 1996. – 175с.
31. Королёв В.А., Некрасова М.А. Экспериментальные исследования электрохимической миграции ионов металлов в дисперсных породах// Геохимия. 1998. № 12. С. 1277-1283.
32. Small M.J. Compounds formed from the chemical decontamination of HD, GB, and VX and their environmental fate. Tech Rpt8304; AD A149515. Fort Detrick, MD:U.S. Army Medical Bioengineering Research and Development Laboratory – 1984.
33. Schowanek D. and Verstraete W. Phosphonate utilization by bacterial cultures and enrichments from environmental samples / Schowanek D. and Verstraete W. //Appl.Environ.Microbiol – 1990.-V. 56.-P. 895-903.
34. Smith J.D. Metabolism of Phosphonates. – In: The role of phosphonates in living systems (Hilderbrand, R.L., ed.) CRC Press, Boca Raton – 1983.-P. 31-54.
35. Selvapandiyan A. and Bhatnagar Raj K. Isolation of glyphosate-metabolising Pseudomonas: detection, partial purification and localization of carbon-phosphorus lyase / Selvapandiyan A. and Bhatnagar Raj K. // Appl. Microbiol. Biotechnol – 1994.-V 40.-P. 876-882.
36. Shinabarger D.L. and Braymer H.D. Glyphosate catabolism by Pseudomonas sp. strain PG2982. / Shinabarger D.L. and Braymer H.D. // J Bacteriol – 1986.-V. 168.-P. 702-703.
37. Shames S.L. Fragmentative and stereochemical isomerisation probes for homolytic carbon to phosphorus bond scission catalysed by bacterial carbon-phosphorus lyase / Shames S.L., Wackett L.P., LaBarge M.S., Kuczkowski R.L. and Walsh C.T. // Bioorg.Chem. – 1987.-V 15.-P. 366-373.
38. Матыс С.В. Деградация метилфосфоната Е. coli: физиологические и биохимические аспекты / Матыс С.В. // Диссертация – 2003. – С. 56.
39. Нифантьев Э.Е. Химия фосфорганических соединений / Нифантьев Э.Е. - М.: 1971.
40. Кононова С.В. и Несмеянова М.А. Фосфонаты и их деградация микроорганизмами / Кононова С.В. и Несмеянова М.А. // Биохимия- 2002.- Т. 67.-С. 220-233.
41. Goldstein A.H., Liu S.T. Molecular cloning and regulation of a mineral phosphate solubilizing gene from Erwinia herbicola – Biotechnology, 1987, v.5 - Р. 72-74.